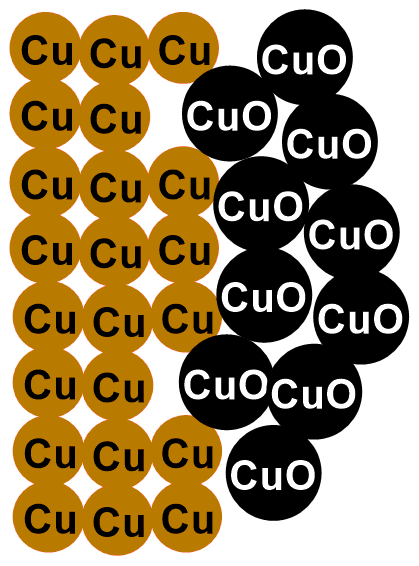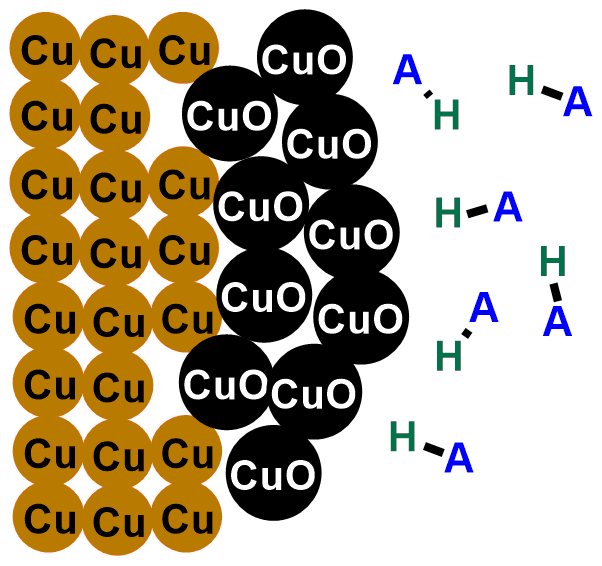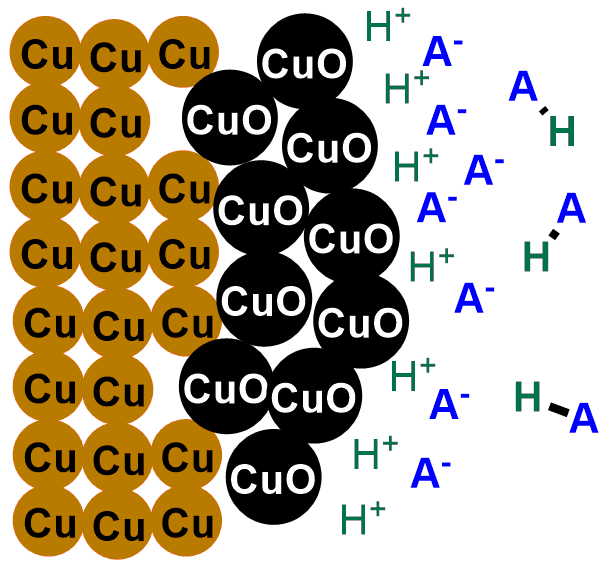Prodotti e strumenti
Per pulire le tue monete hai bisogno dei seguenti prodotti e strumenti:
Prodotti
Strumenti
Tempo
Limone
(o aceto)
Acqua
Monete annerite
Bicchiere
Pinzetta
5 min
Come si vede dalla tabella hai bisogno di un limone e/o aceto di vino e di un po’ di acqua. Riguardo agli strumenti hai bisogno di ciò che normalmente trovi in casa: un bicchiere, monete annerite e una pinzetta.
L’esperimento richiede veramente poco tempo, quindi è adatto anche ai più pigri.
Istruzioni
Le operazioni da fare sono molto semplici:
- Prendi un bicchiere e riempilo di acqua.
- Spremi un limone all’interno del bicchiere con l’acqua.
- Immergici le tue monete annerite per qualche secondo.
- Riprendile con una pinzetta e asciugale con la carta.
Noterai, ora come le monete sono lucenti come appena coniate!
Se, invece del limone e acqua, vorrai usare l’aceto, ricorda che in questo caso, dovrai immergere le tue monete per più tempo prima di vederle pulite.

Vuoi scaricare questo articolo e leggerlo comodamente offline? O ti piacerebbe averlo per modificarlo e usarlo a tuo piacere? Per entrambi i casi, abbiamo la solurione: scarica l’articolo in formato PDF o DOCX qui.
Spiegazione chimica
Come sono fatte la monete
Le monete da 1, 2, 5 centesimi di euro sono fatte per il 95% di acciaio e hanno una placcatura esterna di rame, che contribuisce al restante 5%.
È proprio il rame a dare alle nostre monete l’aspetto rossastro che le contraddistingue. Tuttavia, come sappiamo, le monete con il tempo perdono l’aspetto lucido e vivido e assumono un colore sbiadito e smorto, tanto da divenire completamente nere nei casi più gravi. Dunque ci domandiamo: << Come mai le nostre monete tendono ad ”annerite”? >>.


La reazione di Annerimento
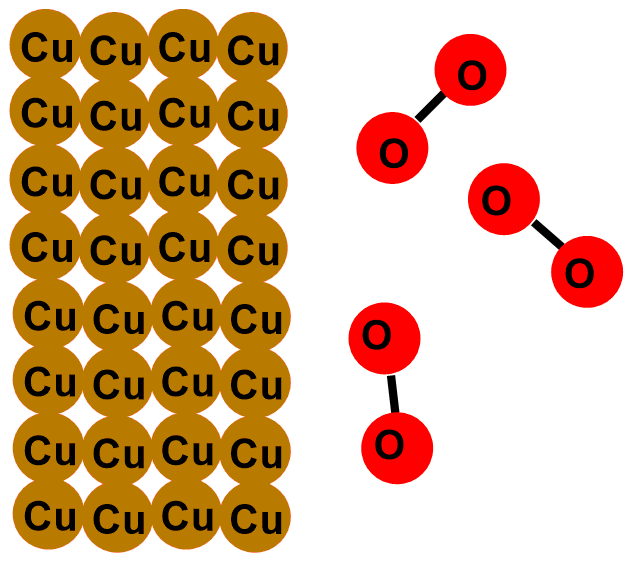
Le monete anneriscono perché il rame (Cu), che costituisce lo strato più esterno della moneta, tende con il tempo a reagire con l’ossigeno (O2) dell’aria, secondo la reazione:
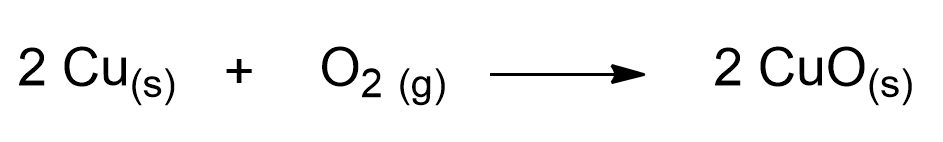
Questa è una reazione detta di ossido-riduzione. In particolare, il rame cede i suoi elettroni all’ossigeno e si trasforma in ossido di rame II (CuO). Tale composto è un solido nero che si stratifica sulle nostre monete. Ecco spiegato perché esse anneriscano con il tempo!
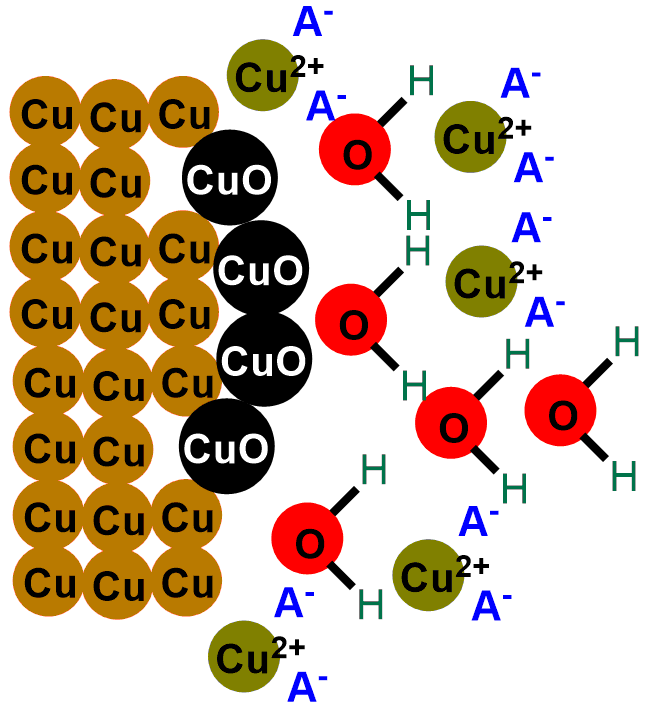
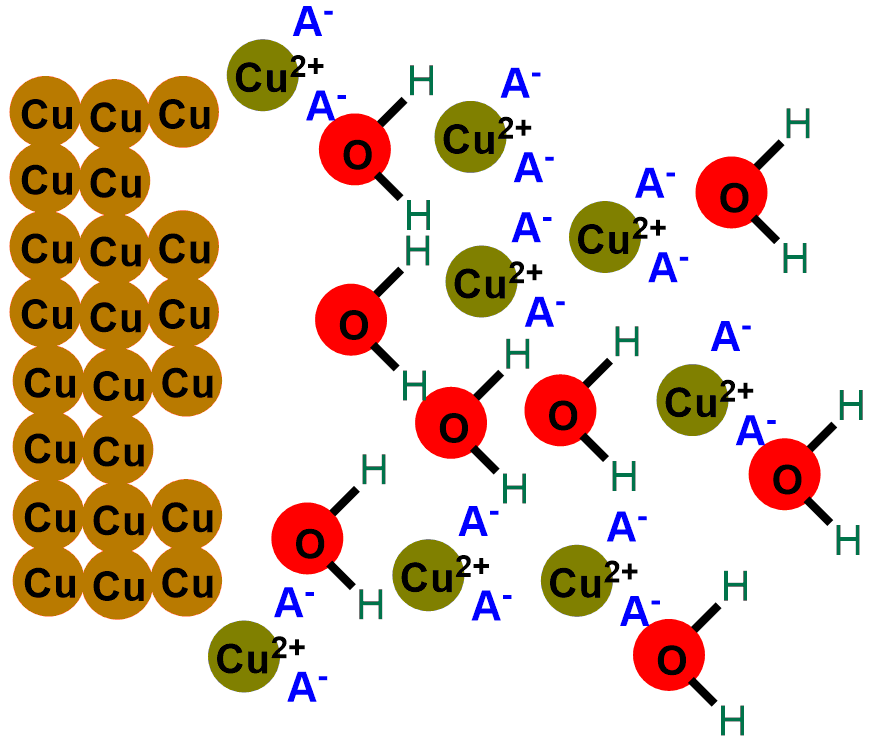
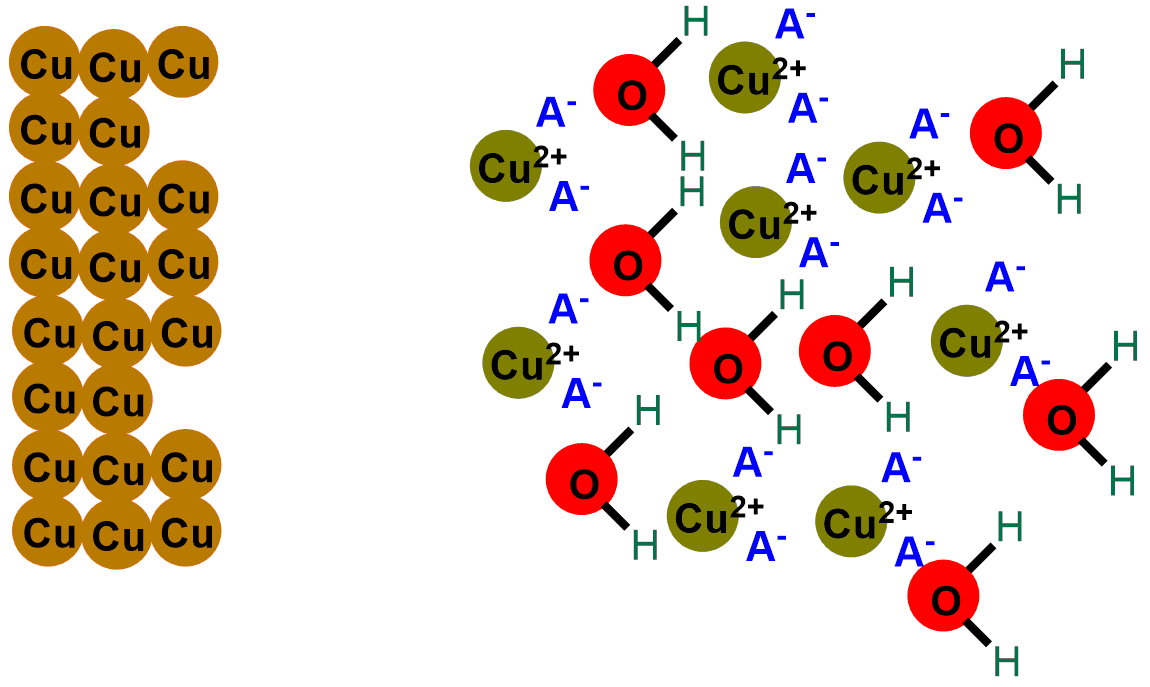
Nelle immagini sottostanti puoi vedere raffigurata la reazione appena descritta. La prima immagine raffigura lo strato più esterno delle monete, che quando sono nuove è composto solo da rame (Cu). Mentre le immagine successive mostrano la formazione dell’ossido di rame per reazione con l’ossigeno.
La reazione di Pulitura
Come facciamo dunque a pulire le nostre monete abbruttite dal nero ossido di rame II?
Abbiamo bisogno di una sostanza che lo distrugga. Questa sostanza è un qualsiasi acido. Se non sai cos’è un acido, non preoccuparti; infatti è sufficiente che tu sappia che un acido, HA, è una sostanza che in soluzione libera ioni H+ e A–, dove H+ sono gli ioni idrogeno carichi positivamente e A– indica una qualsiasi specie carica negativamente, che cambierà a seconda dell’acido usato. Ad esempio, per l’acido cloridrico, HCl, A– è lo ione Cl–, per l’acido solforico di formula H2SO4, A– è SO42- e cosi via. Avrai notato, quindi, che tutti gli acidi hanno in comune lo ione H+ che rilasciano in soluzione.
Dunque quando mettiamo le nostre monete in acido, gli ioni H+ liberati dall’acido reagiscono con l’ossigeno dell’ossido di rame II (CuO) e lo trasformano in acqua (H2O). Mentre lo ione A– acchiappa gli ioni Cu+ portandoli in soluzione. Puoi vedere la reazione che descrive il fenomeno qui sotto:
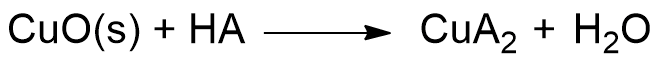
In breve, quello che fa un acido è divorare a poco a poco lo strato di ossido di rame nero, portando in luce nuovamente il rame metallico lucente, dapprima coperto dall’ossido. Se scorri le immagini sottostanti potrai vedere raffigurata la reazione di pulitura delle monete.
Le reazioni specifiche per il limone e aceto
Nell’esperimento indicato in questo articolo abbiamo usato il limone o l’aceto. Perché? Perché entrambi sono acidi.
Infatti il limone contiene l’acido citrico, la cui formula è visibile in basso.
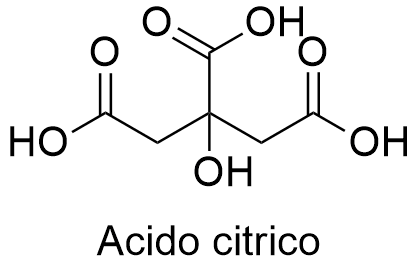
L’acido citrico reagisce con l’ossido di rame, formando citrato di rame e acqua, secondo la reazione:
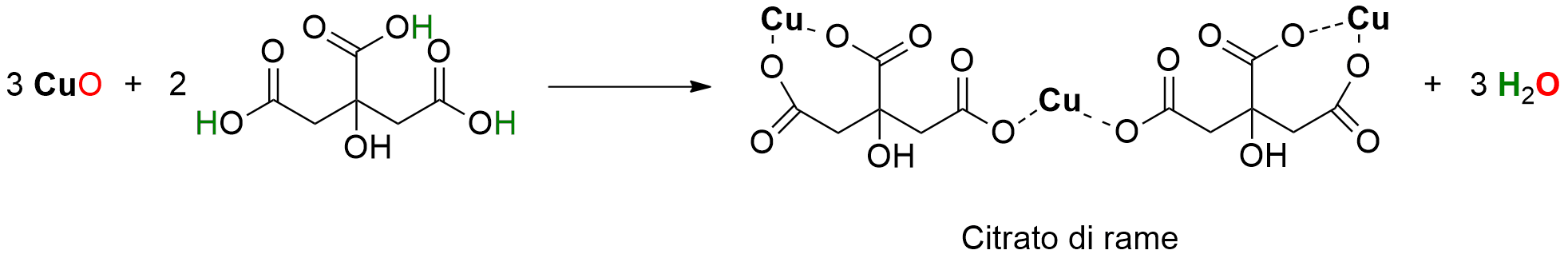
L’aceto invece è una soluzione acquosa che contiene acido acetico, CH3COOH. Tale acido reagisce con l’ossido di rame per formare acetato di rame e acqua, secondo la reazione:
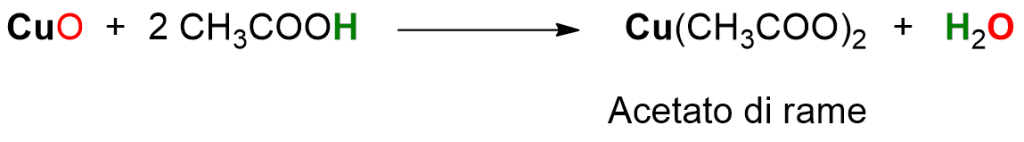
Tuttavia l’aceto ha bisogno di più tempo prima di pulire le nostre monete, mentre il limone è abbastanza immediato. Come mai? Perché l’acido acetico contenuto nell’aceto è meno acido dell’acido citrico del limone e inoltre è presente in quantità basse nell’aceto.
Conclusioni
Con questo esperimento abbiamo imparato i seguenti punti chiave:
- Le nostre monete da 1,2,5 cent sono fatte di uno strato esterno di rame (Cu), che per azione dell’ossigeno, nel tempo, tendono ad annerire, ricoprendosi di uno strato esterno di ossido, CuO (solido nero);
- Possiamo pulire le nostre monete grazie all’azione di un acido, come quello presente nel limone (acido citrico) o nell’aceto (acido acetico). Tale acido agisce ‘mangiando’ a poco a poco lo strato di ossido nero e facendo, così, riaffiorare il rame metallico della moneta. In questo modo la moneta torna lucida e splendente.
Ti è piaciuto questo esperimento e la nostra spiegazione? Faccelo sapere votando questo post in basso o lasciando un commento. Inoltre, se sei curioso di vedere cosa succede alle monete in un acido potentissimo, vedi il nostro video in basso.
Questa lezione

Pulire le monete con la chimica
€
1.50
Scarica pdf (non modificabile)

Pulire le monete con la chimica
€
2.20
Scarica docx (modificabile)