Introduzione
Sei all’inizio dei tuoi studi di Chimica Organica e gli alcheni sono per te di difficile comprensione? Allora questo articolo fa per te! Infatti, con parole semplici e poche chiacchiere questo argomento fumoso diventerà subito chiaro. Inoltre, poichè questo sito nasce per supportare agli studenti, avrai a disposizione i seguenti strumenti come aiuto ulteriore:
Il file pdf o docx di questo articolo, per rileggere gli appunti offline;
Quiz gratuito per testare le tue conoscenze, dopo la lettura dell’articolo;
Mappa concettuale scaricabile, per avere un riassunto visuale dell’intero argomento.
E ora è il momento di iniziare! Armati solo di un po’ di pazienza e fiducia nelle tue capacità! Buona lettura!
Cosa sono gli alcheni?
Gli alcheni sono composti organici costituiti solo da carbonio (C) e idrogeno (H). La loro formula generale è CnH2n, in cui n è un numero intero maggiore o uguale a 2.
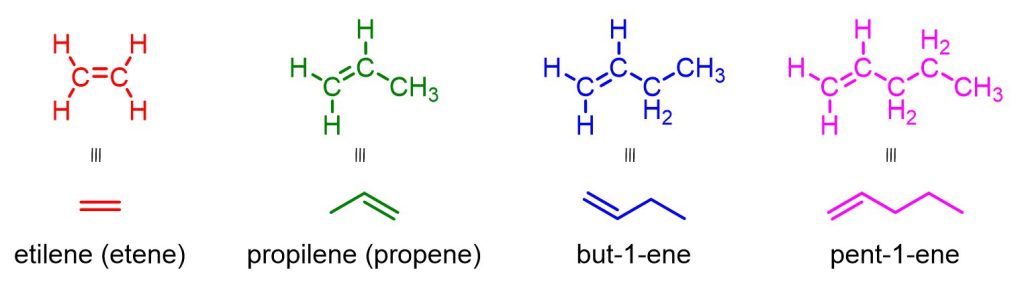
Quindi il primo degli alcheni avrà n=2 e formula generale C2H4 con il nome comune di etilene, anche se la denominazione IUPAC è etene. Segue il propilene (o propene) con formula C3H6, il but-1-ene con formula C4H8, il pent-1-ene con formula C5H10 e così via. La figura in basso illustra questi primi quattro alcheni più semplici.
La nomenclatura degli alcheni
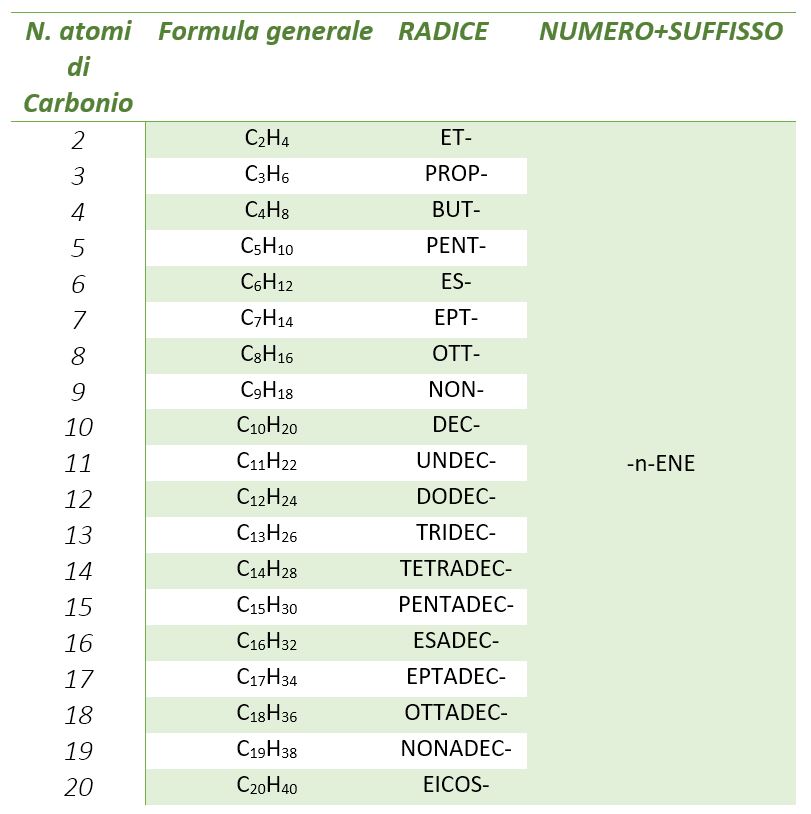
La nomenclatura degli alcheni non è molto diversa da quella degli alcani. Infatti la prima parte del loro nome, la radice, è identica a quella degli alcani e identifica il numero totale di atomi di carbonio. Per 2 atomi di carbonio la radice è ET-, per 3 PROP-, per 4 BUT-, mentre a partire da 5 atomi di carbonio la radice deriva dal prefisso numerale greco. La tabella sottostante elenca tutte le radici da 2 a 20.
La nomenclatura degli alcheni, tuttavia, si distingue da quella degli alcani per tre ragioni:
Sei sicuro di aver capito come chiamare gli alcheni? Se ancora sei confuso, ti propongo degli esercizi svolti in basso che mettono la teoria in azione. Se, invece, pensi di aver capito tutto, prova gli esercizi in autonomia.
Esercizi svolti
Nota: Se hai dubbi sulla nomenclatura delle molecole organiche più complesse, prova il nostro articolo completo ”Tutta la Nomenclatura dei Composti Organici ” che tratta la nomenclatura organica tutta insieme, fornendo un quadro completo e definitivo dell’argomento.
Nomenclatura tradizionale
Alcuni alcheni mantengono ancora oggi una nomenclatura diversa da quella IUPAC, detta ‘’nomenclatura tradizionale’’, perché affonda le sue origini da un linguaggio comune usato dagli scienziati in un periodo antecedente allo sviluppo di una nomenclatura sistematica e universale. Tuttavia la nomenclatura tradizionale è ancora molto usata e quindi occorre impararla per poter comunicare bene con i chimici, specie con quelli più anzianotti!
Nella tabella seguente trovi i nomi tradizionali più usati per gli alcheni, affiancati dalla corrispondente denominazione IUPAC.
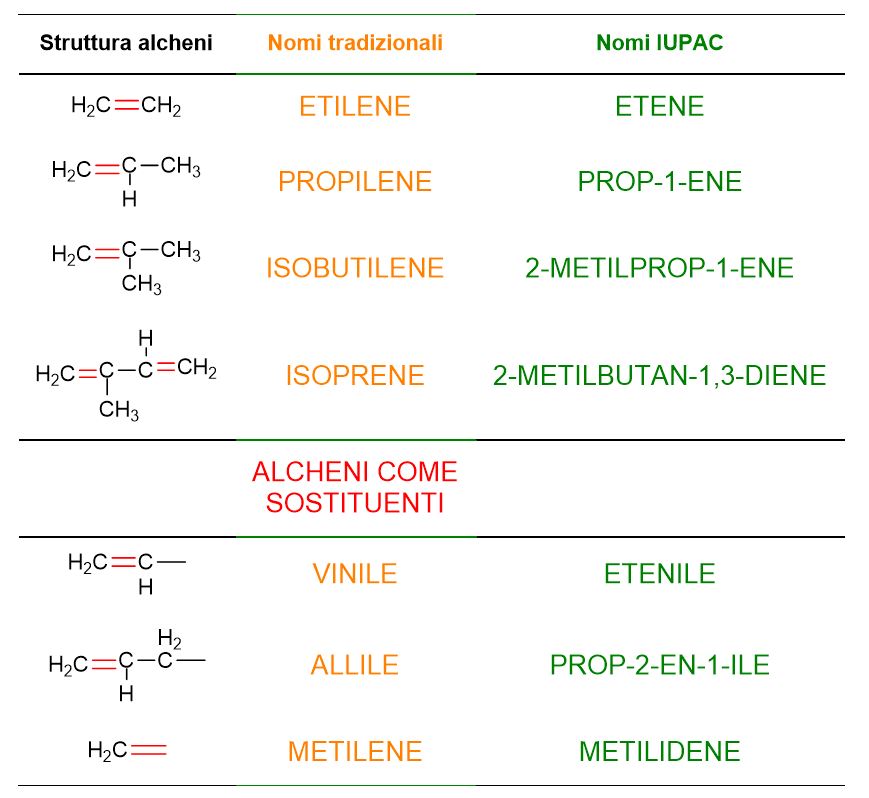
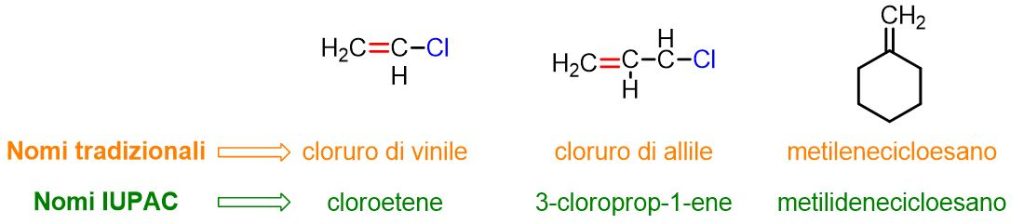
Nelle ultime 3 righe della Tabella 2, sono riportati alcuni esempi di nomi tradizionali per alcheni sostituenti. Tali nomi possono essere impiegati per indicare alcune olefine, come si può vedere nella figura in basso.
Ibridazione degli alcheni
Nell’articolo alcani abbiamo imparato che gli atomi di carbonio di queste molecole sono tutti ibridati sp3.
Ma qual è l’ibridazione degli alcheni?
In realtà tutti gli atomi di carbonio di un alchene che NON sono coinvolti nel doppio legame, continueranno ad avere ibridazione sp3 e quindi geometria tetraedrica. L’ibridazione cambia solo per gli atomi di carbonio coinvolti nel doppio legame. Questi infatti avranno ibridazione sp2.
Ma cosa vuol dire? Ricordiamo la configurazione elettronica del carbonio. Esso ha due elettroni nell’orbitale 2s e due negli orbitali p. Tuttavia affinché l’atomo di carbonio possa formare quattro legami, uno degli elettroni dell’orbitale s, viene promosso nell’orbitale vuoto p. Vedi la figura animata sottostante.

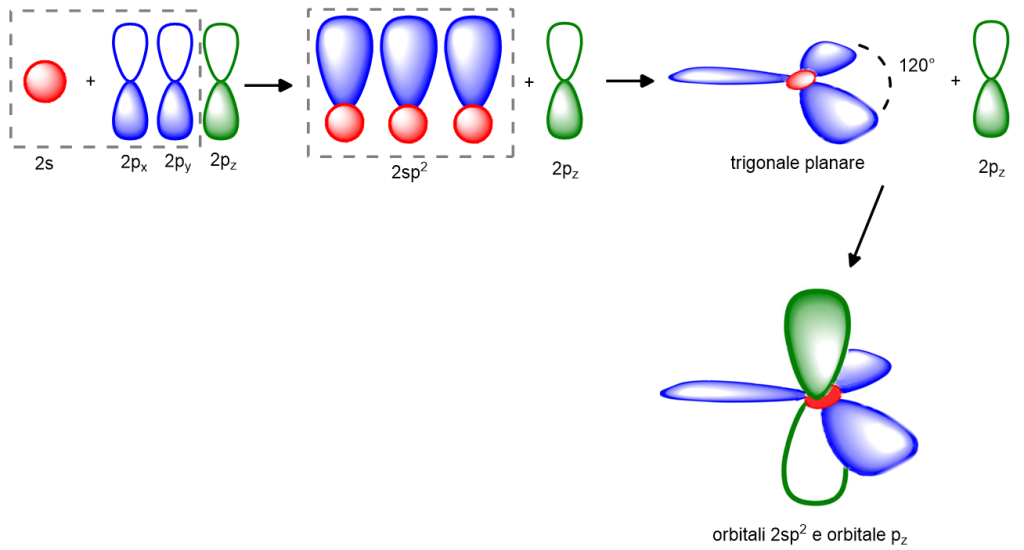
A questo punto ci sono quattro elettroni spaiati negli orbitali s e p. Tali orbitali per formare il doppio legame si ibridano, ossia si fondono insieme per formare un nuovo assetto di orbitali, in grado di dar vita al doppio legame. A differenza dell’ibridazione sp3, dove tutti e quattro gli orbitali si fondevano tra loro, nell’ibridazione sp2, sono solo tre gli orbitali ad ibridarsi (un orbitale s e due orbitali p, px e py), mentre l’altro (l’orbitale pz) resta invariato. Nel momento in cui questi tre orbitali si ibridano, cambiano la loro forma per assumerne una che rispecchia il carattere di tutti e tre gli orbitali che si mescolano. Ora siccome l’orbitale s è sferico, mentre quelli p sono bilobati, gli orbitali risultanti dal mescolamento di un orbitale s e due orbitali p, hanno una forma intermedia tra quella sferica e quella bilobata. Vedi gli orbitali sp2 nell’immagine sottostante.
Tali orbitali ibridi assumono una posizione planare nello spazio con angoli di 120° tra un orbitale e l’altro. L’orbitale pz, che non si è fuso con gli altri, resta identico a se stesso e giacerà sopra e sotto il piano degli orbitali ibridi sp2 (ultima immagine in Figura 4).
Ma come si forma di fatto il doppio legame?
Facciamo interagire tra loro due atomi di carbonio ibridi sp2. Uno degli orbitali sp2 di un atomo di carbonio interagisce con un orbitale sp2 dell’altro atomo di carbonio, per formare un orbitale di legame di tipo σ (in blu in Figura 5). L’orbitale σ ha simmetria cilindrica rispetto all’asse che congiunge i due nuclei di carbonio. In altre parole tale orbitale è una specie di salsicciotto che si estende intorno all’asse immaginario che passa per i due nuclei interagenti. Tuttavia, entrambi gli atomi di carbonio hanno anche un orbitale pz non ibrido. Gli orbitali pz non ibridi interagiscono lateralmente tra di loro, creando un orbitale molecolare di legame di tipo π, con densità elettronica sopra e sotto il piano xy.
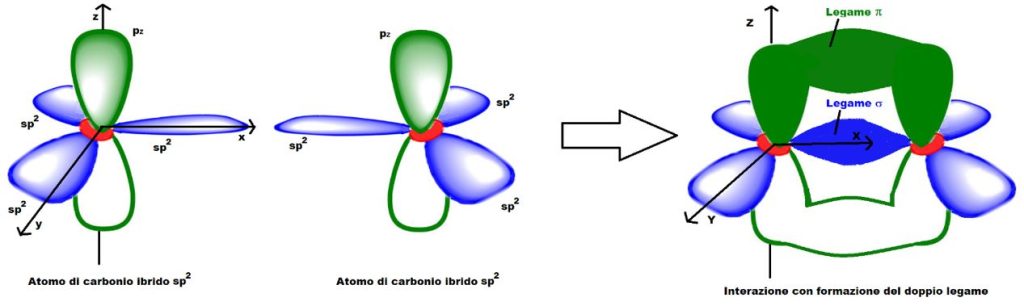
L’orbitale π è di fatto l’orbitale responsabile della formazione del doppio legame negli alcheni. Rispetto a un orbitale σ, risulta meno forte perché presenta un nodo proprio lungo l’asse che passa tra i due nuclei interagenti e nasce da due orbitali che si sovrappongono solo lateralmente e solo in due punti.
Tuttavia il doppio legame tra due atomi di carbonio è nel complesso più forte di un legame singolo C-C, perché i due nuclei sono uniti sia tramite legame σ sia tramite legame π, mentre il legame C-C singolo è formato da un solo legame σ.
Cosa ne sarà degli altri due orbitali ibridi sp2 presenti su ciascun carbonio? Questi orbitali possono essere impiegati per formare altri legami σ con altri atomi di carbonio o con idrogeni.
Per esempio nell’etilene (C2H4) gli orbitali ibridi sp2, non coinvolti nella formazione del doppio legame, interagiscono ciascuno con un orbitale s di un atomo di idrogeno, tramite interazioni σ (Figura 6).
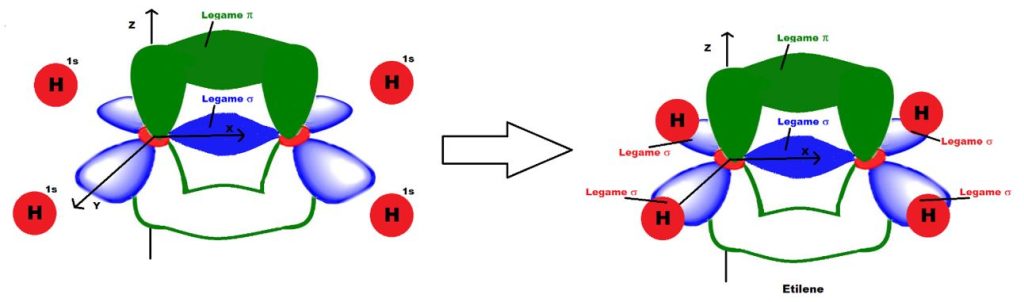
Distanza di legame
Il doppio legame C=C degli alcheni ha una lunghezza inferiore rispetto al legame singolo C-C degli alcani. Questo perché nel doppio legame la presenza congiunta del legame π e del legame σ aggiunge densità elettronica tra i due nuclei di carbonio, rispetto alla densità dovuta al solo legame σ degli alcani.
Se prendiamo come esempio di nuovo la molecola di etilene vediamo che la distanza di legame C=C è di 1.34 Å (Figura 7), mentre quella del legame C-C dell’alcano corrispondente (l’etano) è di 1.54 Å. Tuttavia se confrontiamo anche la lunghezza dei legami C-H tra etilene ed etano, ci accorgiamo che anche questi legami sono più corti nell’etilene (1.09 Å vs 1.10 Å).
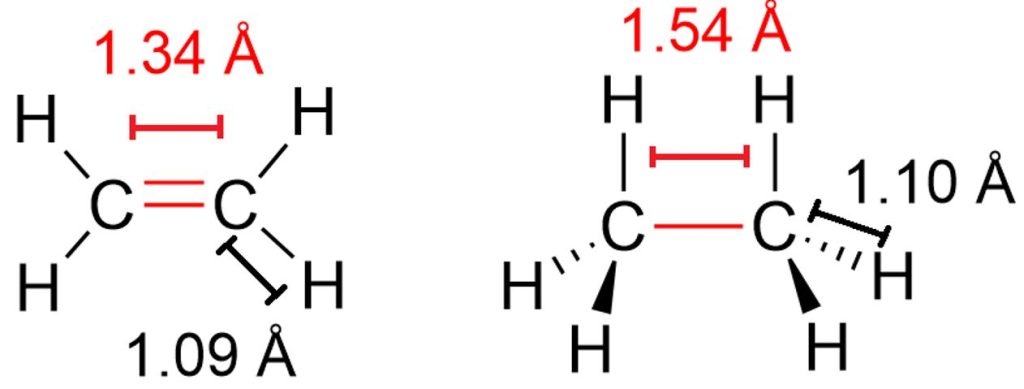
La riduzione della lunghezza dei legami σ dei 2 atomi di carbonio coinvolti nel doppio legame, è una caratteristica costante negli alcheni ed è dovuta all’ibridazione sp2 degli stessi atomi. Infatti l’ibridazione sp2 rispetto a quella sp3, comporta un maggior contributo dell’orbitale s all’ibrido risultante, poiché a interagire sono 1 orbitale s e 2 orbitali p. Contrariamente nell’ibridazione sp3 il contributo dell’orbitale s è inferiore dato che l’interazione è data da 1 orbitale s e 3 orbitali p. Siccome l’orbitale s ha una densità elettronica molto vicina al nucleo, il maggiore carattere s negli orbitali ibridi sp2, fa sì che tali orbitali siano più concentrati intorno ai nuclei rispetto agli orbitali sp3. Questo di conseguenza comporta una riduzione di tutte le lunghezze dei legami σ che si formano con un atomo di carbonio ibrido sp2.
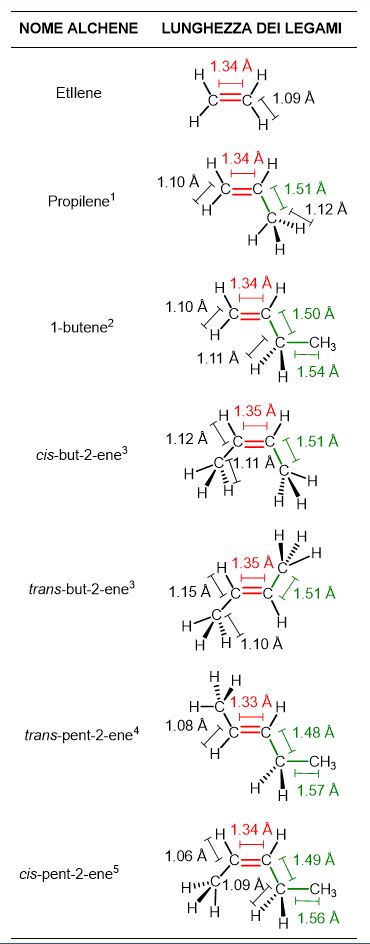
Le lunghezze di legame per i primi 4 alcheni sono riportate nella Tabella 3 di seguito. Generalmente la lunghezza tipica del (sp2)C=C(sp2) è intorno a 1.34-1.35 Å, mentre quella di un (sp3)C-C(sp3) si aggira intorno a 1.54-1.57 Å. Leggermente più corte sono le distanze tra (sp2)=C-C(sp3)con valori compresi tra 1.48-1.51 Å.[1-5]
Isomeria cis/trans
La presenza del doppio legame negli alcheni genera una particolare isomeria che non era presente, invece, negli alcani semplici. Questa isomeria è nota come isomeria geometrica e prevede di distinguere tra due isomeri: l’isomero cis e l’isomero trans.
In particolare, la presenza del doppio legame rende la molecola rigida in quel punto, ossia incapace di ruotare. Mentre intorno a un legame C-C singolo vi è libera rotazione a temperatura ambiente, intorno a un legame C=C questa rotazione è impedita dalla presenza del legame π aggiuntivo. Per far sì che un C=C ruoti occorrerebbe quindi rompere il legame π, cosa che può avvenire solo a temperature molto alte (circa 300°C), in condizioni acide o tramite fotocatalisi. È proprio tale rigidità del legame C=C a rendere possibile l’isomeria cis e trans.
Ma cosa sono questi isomeri cis e trans? Vediamolo con un esempio.
Prendiamo il primo alchene che presenta tale isomeria, ossia il but-2-ene. Dall’immagine sottostante è possibile vedere che l’isomero cis del but-2-ene, ha i due H tutti e due dallo stesso lato, e lo stesso si può dire dei due gruppi CH3. Nell’isomero trans invece i due H sono da parti opposte, così come i due gruppi CH3.
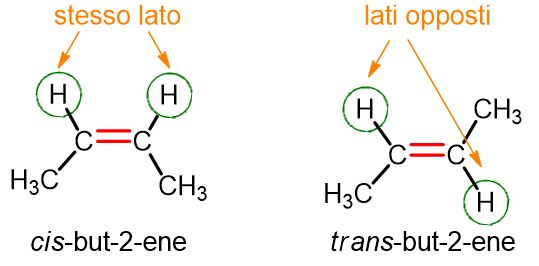
Nel caso di alcheni bisostituiti, come il but-2-ene (quindi con un idrogeno e un sostituente su ogni carbonio coinvolto nel doppio legame) possiamo dire che:
l’isomero cis (o Z) è quello con i due idrogeni (o i due sostituenti) dallo stesso lato;
l’isomero trans (o E) è quello con i due idrogeni (o i due sostituenti) da parti opposte.
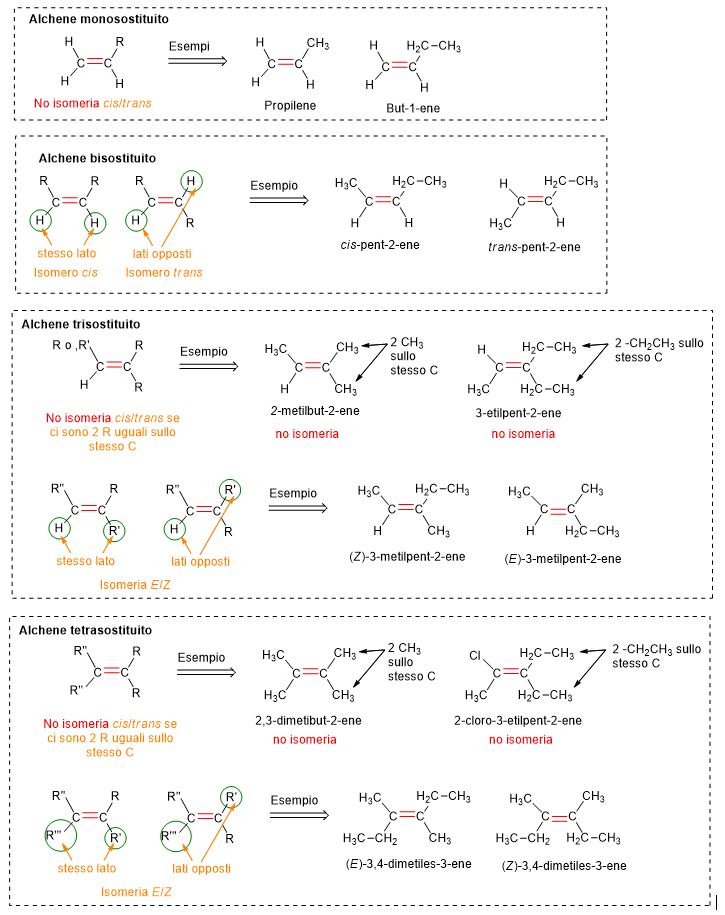
Non tutti gli alcheni presentano tale isomeria, più specificamente gli alcheni:
Monosostituiti non presentano mai isomeria cis–trans;
Tri- e tetra-sostituiti la presentano in quasi tutti i casi tranne nel caso in cui ci siano 2 sostituenti uguali sullo stesso atomo di carbonio coinvolto nel doppio legame.
L’immagine che segue chiarisce questi concetti con degli esempi pratici. É bene notare che nel caso di alcheni tri-sostituiti e tetra-sostituiti la nomenclatura cis/trans è difficilmente applicabile, perciò si preferisce quella E/Z, che prevede delle regole specifiche per assegnare i due isomeri. Non vedremo tali regole in questo articolo, ma presto metterò a disposizione un articolo specifico per questo argomento.
Stabilità degli alcheni
Nell’immagine sottostante è riportata una scala generica di stabilità degli alcheni. Si possono cogliere le seguenti informazioni:
gli alcheni tetrasostituiti sono più stabili dei trisostituiti;
gli alcheni trisostituiti sono più stabili dei disostituiti;
tra gli alcheni disostituiti l’isomero trans è sempre più stabile del cis;
gli alcheni disostituiti sono più stabili dei monosostituiti;
gli alcheni monosostituiti sono più stabili dell’etilene (ossia alchene non alchilato).
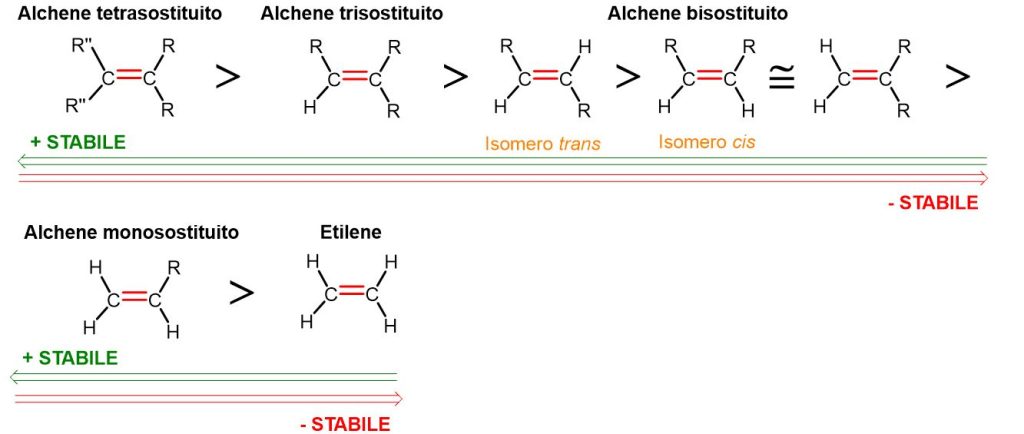
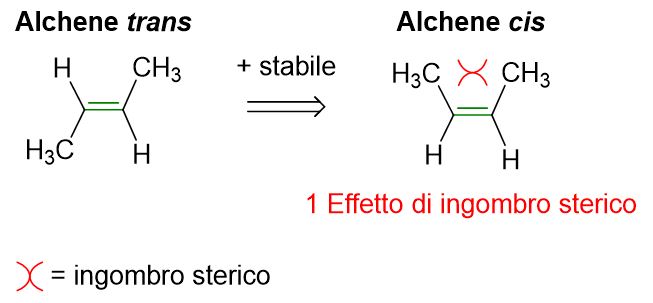
Quindi in generale possiamo ricavare la seguente regola: l’alchene più sostituito è più stabile di uno meno sostituito e l’alchene trans è più stabile del cis.
Ma a cosa è dovuto questo andamento? Vediamo prima perché un alchene più sostituito è più stabile di uno non sostituito.
Questo è dovuto a una ragione essenziale: l’alchene più sostituito ha più gruppi R alchilici vicino al doppio legame, questo comporta un rilascio di densità elettronica dai gruppi R (ricchi di elettroni e con ibridazione sp3 dei carboni) ai carboni del doppio legame ibridi sp2, che sono più elettronegativi dei carboni sp3 (vedi Figura 11).
Questo fenomeno noto come iperconiugazione, coinvolge in realtà una sovrapposizione degli orbitali molecolari, cosa che spiegherò più in dettaglio in un articolo a parte. Ad ogni modo la spiegazione fornita sopra è più che sufficiente per rispondere in modo esaustivo a una domanda nel merito durante un esame di Chimica Organica I.
È importante altresì notare che, nonostante il maggiore ingombro sterico degli alcheni più sostituiti, l’effetto iperconiugativo compensa così bene le repulsioni steriche da rendere un alchene tetralchilato, e quindi molto ingombrato, notevolmente più stabile di un alchene monoalchilato, dove, invece, le repulsioni steriche sono minime.
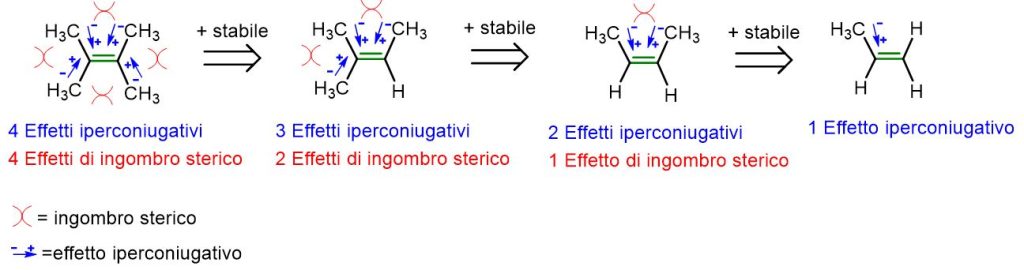
Concludiamo questo paragrafo spiegando la maggiore stabilità dell’isomero trans rispetto al cis. In questo contesto, la spiegazione più semplice e accettata è che i due gruppi R del cis essendo molto vicini tra loro tendono a respingersi e quindi a destabilizzare l’intera molecola. Diversamente, i medesimi gruppi R sul trans sono più distanti tra di loro e quindi non manifestano alcuna repulsione.
Proprietà fisiche degli alcheni
Gli alcheni hanno proprietà fisiche simili agli alcani: sono anch’essi molecole apolari e insolubili in acqua. Risultano solubili in solventi some etere etilico, alcoli, esano, etc..
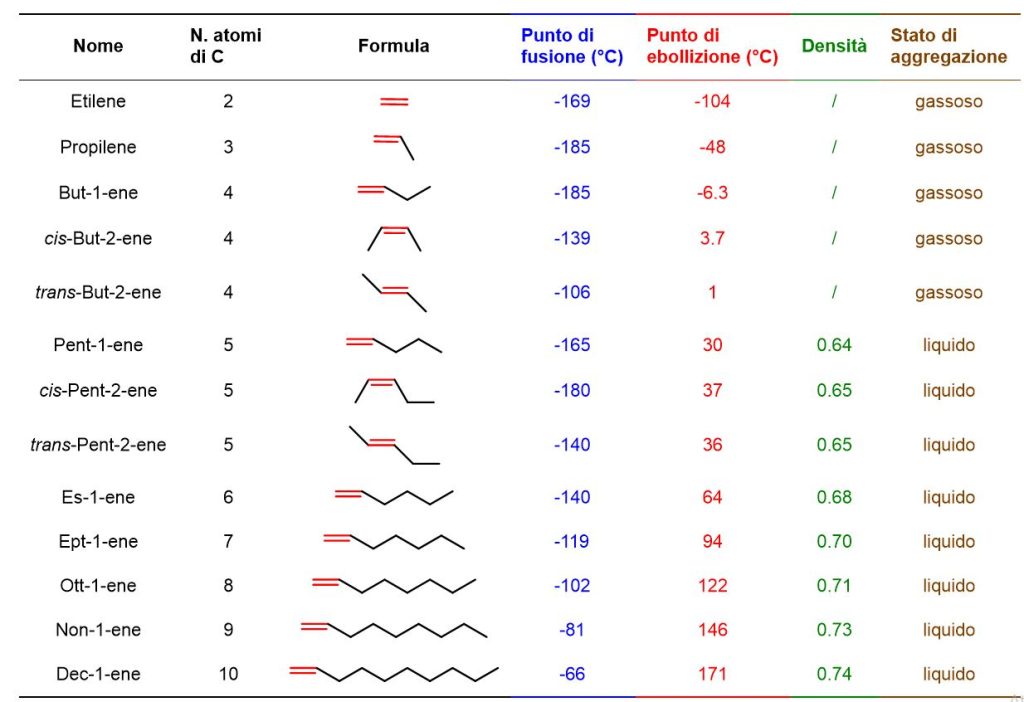
I primi 3 alcheni (etilene, propilene e butene) sono gassosi, gli altri fino a C20H40 sono liquidi incolori con densità inferiore a quella dell’acqua. Gli alcheni successivi sono, invece, solidi.
I punti di ebollizione aumentano generalmente con la lunghezza della catena, ma dipendono anche dalla forma della molecola e dal tipo di isomeria. A tal proposito si possono vedere i vari esempi riportati in Tabella 4. Confrontando i punti di ebollizione degli 1-alcheni, è evidente che, passando dall’etilene con 2 atomi di C al 1-decene con 10 atomi di C, il punto di ebollizione aumenta vertiginosamente passando da -104°C dell’etilene a 171°C dell’1-decene.
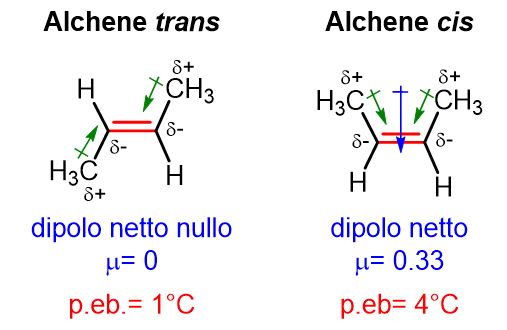
Per quanto riguarda l’isomeria cis–trans, gli alcheni cis hanno generalmente punti di ebollizione più alti degli alcheni trans. Questo fenomeno è dovuto al fatto che gli alcheni trans sono meno polari dei cis. Infatti i momenti di dipolo, che si creano in seguito all’effetto iperconiugativo di rilascio elettronico dai sostituenti R ai carboni sp2 del doppio legame, si annullano nell’isomero trans, perché i vettori dipolari hanno la stessa direzione ma verso opposto, quindi la polarità totale della molecola trans risulta nulla. Lo stesso non avviene nel cis, dove invece, i momenti di dipolo si sommano e la molecola risulta polare. Vedi un esempio in Figura 13.
Reattività degli alcheni
Gli alcheni danno principalmente vita a due classi di reazioni: l’addizione elettrofila e la polimerizzazione. Entrambe coinvolgono il doppio legame direttamente.
Vediamole entrambe in modo schematico, per avere un quadro generale.
Addizione elettrofila: quadro generale
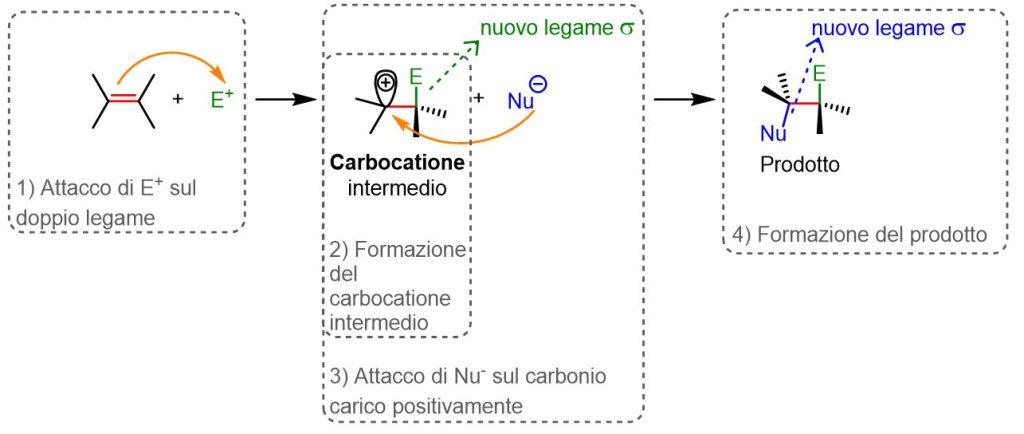
Il doppio legame è un centro ricco di elettroni, dunque le molecole elettrofile (molecole con deficienza elettronica) saranno attratte verso il doppio legame. L’addizione elettrofila coinvolge, infatti un elettrofilo (E+) che attacca il doppio legame (Punto 1, Figura 14). Si rompe così il doppio legame e si forma un intermedio di reazione con un nuovo legame σ tra E+ e uno degli atomi di carbonio coinvolto nel doppio legame. Tale intermedio, inoltre, reca una carica positiva sull’altro atomo di carbonio che non ha reagito con E+, perché ora tale carbonio formerà solo 3 legami e non i 4 tipici della sua valenza. L’intermedio in questione è pertanto chiamato CARBOCATIONE (Punto 2, Figura 14). Successivamente il carbocatione reagisce con un nucleofilo (Nu, molecola ricca di elettroni), che attirato dalla carica positiva, forma un legame σ con il carbonio carico positivamente (Punto 3, Figura 14). Si forma il prodotto della reazione che è una molecola satura, dove il doppio legame è stato sostituito da 2 nuovi legami σ (Punto 4, Figura 14).
Polimerizzazione
Se non sono presenti nucleofili durante la reazione di addizione elettrofila, sarà l’alchene stesso, che non ha reagito, ad agire da nucleofilo e a dare luogo alla reazione di polimerizzazione degli alcheni. Questo è possibile perché il doppio legame ת degli alcheni è un centro ricco di elettroni, quindi di fatto può agire da nucleofilo.
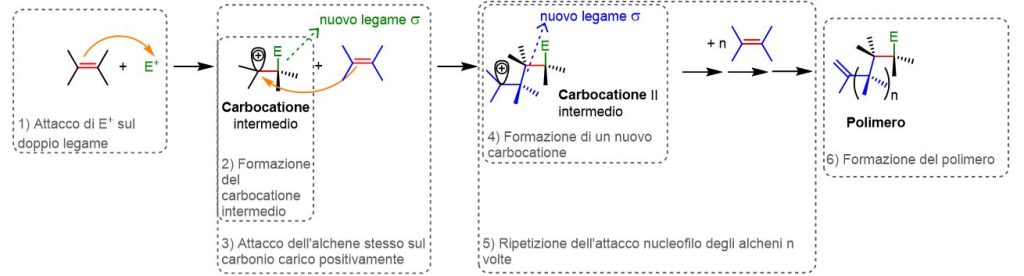
Più in dettaglio, dopo l’attacco di un elettrofilo al doppio legame (Punto 1, Figura 15) e la formazione del carbocatione (Punto 2, Figura 15), nella polimerizzazione è un’altra molecola di alchene a reagire con il carbocatione (Punto 3, Figura 15). In questo modo si forma un nuovo carbocatione (Punto 4, Figura 15) che potrà reagire di nuovo a sua volta con una molecola di alchene e così via (Punto 5, Figura 15). Il processo si ripete numerose volte producendo un polimero (Punto 6, Figura 15), ossia una molecola con massa molecolare elevata dove delle strutture molecolari si ripetono con regolarità per tutta la lunghezza del polimero.
Conclusioni
In questo articolo ti ho fornito un riassunto veloce ma completo sugli alcheni, trattandone la nomenclatura, l’ibridazione, l’isomeria cis–trans, la stabilità, le proprietà fisiche e la reattività.
Se le troppe informazioni ti stanno confondendo, niente paura! 💡
Puoi mettere alla prova ciò che hai imparato con il nostro quiz gratuito sugli alcheni, perfetto per ripassare in modo interattivo e divertente.
Preferisci studiare con calma? 📚
Scarica il file PDF o DOCX di questo articolo e leggilo comodamente anche offline.
E per fissare davvero i concetti nella memoria a lungo termine, prova la nostra mappa concettuale sugli alcheni: un modo pratico ed efficace per memorizzare e riassumere!⚗️
Riferimenti
1) Tokue, I.; Fukuyama, T.; Kuchitsu, K. Molecular Structures of Propene and 3,3,3-Trifluoropropene Determined by Gas Electron Diffraction. Journal of Molecular Structure 1973, 17 (2), 207–223. https://doi.org/10.1016/0022-2860(73)85164-6.
2) Van Hemelrijk, D.; Van Den Enden, L.; Geise, H. J.; Sellers, H. L.; Schaefer, L. Structure Determination of 1-Butene by Gas Electron Diffraction, Microwave Spectroscopy, Molecular Mechanics, and Molecular Orbital Constrained Electron Diffraction. J. Am. Chem. Soc. 1980, 102 (7), 2189–2195. https://doi.org/10.1021/ja00527a007
3) Almenningen, A.; Anfinsen, I. M.; Haaland, A. Electron Diffraction Studies of cis– and trans-2-Butene. Acta Chem. Scand. 1970, 24, 43–49.
4) Ter Brake, J. H. M.; Mijlhoff, F. C. Trans-Pent-2-Ene. Electron Diffraction, Vibrational Analysis and Molecular Mechanics. Journal of Molecular Structure 1981, 77 (3–4), 253–263. https://doi.org/10.1016/0022-2860(81)80069-5.
5) Ter Brake, J. H. M. Cis-Pent-2-Ene. Electron Diffraction, Vibrational Analysis and Molecular Mechanics. Journal of Molecular Structure 1984, 118 (1–2), 63–71. https://doi.org/10.1016/0022-2860(84)85180-7.
Questa lezione

Gli alcheni-La nostra guida
€
4.00
Scarica pdf (non modificabile)

Gli alcheni-La nostra guida
€
5.00
Scarica docx (modificabile)

Gli alcheni-La nostra mappa concettuale
€
4.50
Scarica il pdf e stampa la tua mappa!