Introduzione
Sei uno studente alle prime armi con il laboratorio di Chimica Organica e non hai capito proprio nulla della lezione tediosa tenuta dai tuoi professori? Non preoccuparti grazie a questo articolo e ai materiali che ti metto a disposizione (pdf scaricabili, video-tutorial e corso completo sul laboratorio di Chimica Organica) potrai capirci sicuramente molto di più. In questo articolo parliamo in particolare di TLC (Thin Layer Chromatography) una tecnica molto comune, semplice ed utile.
Definizione
La TLC è la cromatografia su strato sottile (dall’inglese Thin Layer Chromatography). Per capire dunque cos’è una TLC occorre capire il significato delle due parole chiave che la compongono: cromatografia e strato sottile.
Def. Cromatografia
La cromatografia è una tecnica di purificazione di una miscela di sostanze attraverso la loro diversa interazione con una fase mobile (liquido, gas o fluido) e una fase stazionaria (solido o liquido) posta su un opportuno supporto.
Dalla definizione si capisce chiaramente che la cromatografia serve per purificare i composti. Meno chiaro potrebbe essere il come si riesce a purificare. Chiariremo meglio questo punto quando, più avanti nell’articolo, vedremo come funziona una TLC; per ora ti basti sapere che in cromatografia per purificare occorrono sempre due fasi: la fase stazionaria e la fase mobile.

Vuoi leggere la nostra guida passo-passo su come effettuare una TLC in laboratorio? Puoi scaricare il pdf o il file docx che riassume sia teoria che pratica sulle TLC. Trovi il file alla fine di questo articolo
Classificazione
Esistono vari tipi di cromatografie, ragione per cui sono state create varie classificazioni per razionalizzare questa varietà. Ad esempio esiste una classificazione in base al tipo di fase mobile usata (es. gas cromatografia, dove la fase mobile è un gas o cromatografia liquida, dove la fase mobile è un liquido), ma anche una classificazione in base al tipo di interazione soluto-fase stazionaria (es. cromatografia di adsorbimento, cromatografia di ripartizione, cromatografia a scambio ionico, cromatografia su setaccio molecolare).
La TLC fa parte della cromatografia liquida, perché usa come fase mobile una miscela di solventi, e della cromatografia di adsorbimento.
Con il termine cromatografia di adsorbimento ci si riferisce a una cromatografia dove l’interazione soluto-fase stazionaria avviene alla superficie della fase stazionaria mediante interazioni varie (legami idrogeno, interazioni dipolo-dipolo, interazioni di van der Waals). La parola adsorbimento, non va confusa con assorbimento, la prima infatti si riferisce a un’interazione con la sola superficie di una sostanza, mentre la seconda parola fa riferimento a un’interazione con tutto il volume di una sostanza.
La cromatografia di adsorbimento si suddivide in due ulteriori categorie a seconda del supporto usato per la fase stazionaria:
Cromatografia su colonna, dove la fase stazionaria è inserita all’interno di una colonna di vetro;
Cromatografia su strato sottile, dove la fase stazionaria è depositata come strato sottile su un supporto di vetro, alluminio o plastica.
Dunque abbiamo finalmente capito le due parole chiavi che compongono il nome TLC, ossia cromatografia e strato sottile. Passiamo ora a vedere come è fatta materialmente.
TLC
Come è fatta una TLC
Dunque, come è fatta una TLC? La TLC è una lastra su cui è depositato il materiale adsorbente (la fase stazionaria), spesso mischiato a un legante (gesso, amido solubile, ecc.) per conferire compattezza al materiale. Oltre al legante, la fase stazionaria è spesso anche miscelata con un indicatore fluorescente che servirà in fase di rivelazione della TLC. La fase stazionaria si trova quindi depositata, insieme ad altri materiali, su un supporto sottile che può essere vetro, alluminio, plastica.
Per un esempio di TLC puoi vedere la figura sottostante, che mostra una TLC 20 x 20 cm su supporto in vetro.
Dalla descrizione di una TLC si capisce subito che sono disponibili vari modelli di TLC sul mercato, in base a dimensione, tipo di fase stazionaria, tipo di supporto.
In particolare, oltre alla TLC 20×20 cm, esistono TLC più piccole di dimensione per esempio 5×10 cm. La dimensione ideale dipende dall’uso che se ne vuole fare. Ad esempio la 20×20 cm è impiegata per purificare, direttamente su lastra, piccole quantità di campione (20-50 mg) o, in alternativa, può essere tagliata per ottenere delle TLC più piccole. La TLC 5×10 cm, invece è impiegata solitamente per scopi analitici.
Tuttavia ciò che deve maggiormente guidare nella scelta di una TLC è la fase stazionaria, perché da essa dipenderà la bontà della separazione dei composti. Esistono varie fasi stazionarie, ma le più comuni sono certamente gel di silice, allumina, florisil, cellulosa, amido.
Come funziona una TLC
Dopo aver visto come è fatta una TLC, non resta che capire come funziona.
La TLC viene eseguita mediante le seguenti fasi:
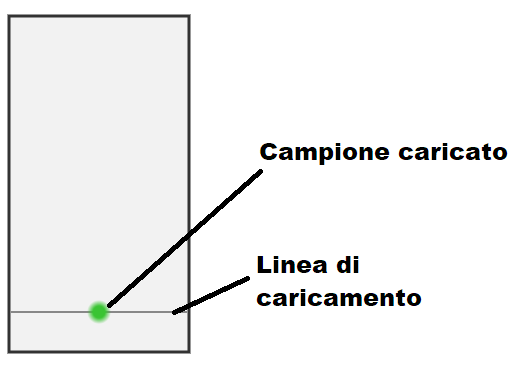
1) Puntare il campione, opportunamente diluito in un solvente, sulla zona di caricamento della TLC. Questa zona è una linea precedentemente disegnata a matita a 7-8 mm dal fondo della TLC. Il campione viene puntato mediante l’ausilio di capillari, ossia tubi di vetro dal diametro piccolo che raccolgono i liquidi per capillarità. Il caricamento del campione deve essere eseguito in modo da creare un piccolo cerchio dal diametro non superiore ai 2 mm.
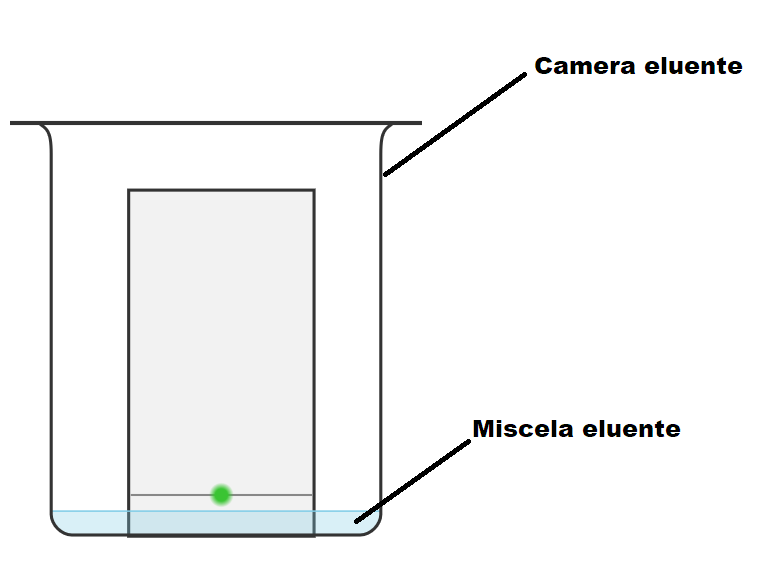
2) Inserire la TLC nella camera di eluizione e aggiungervi la miscela eluente. La camera di eluizione è un contenitore che può essere chiuso alla sommità con un coperchio (ad es. un barattolo). In tale camera viene inserita la TLC insieme a una miscela di solventi, che costituisce la fase mobile (anche detta eluente).
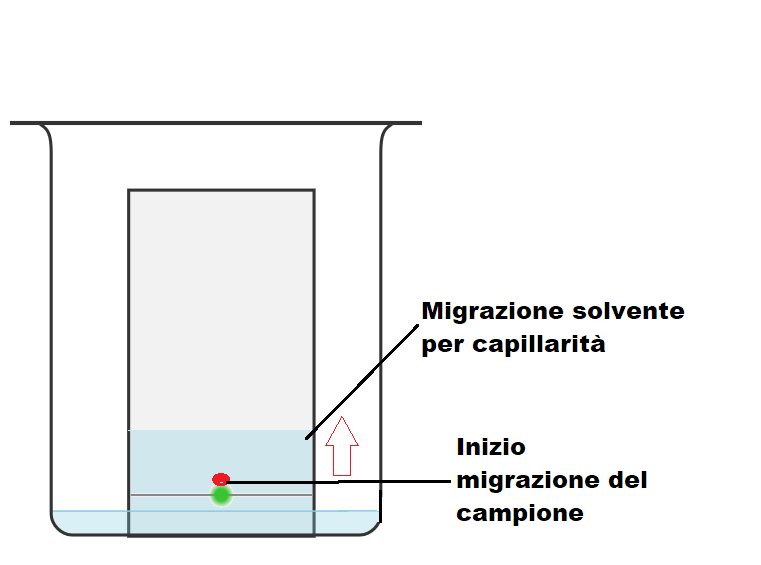
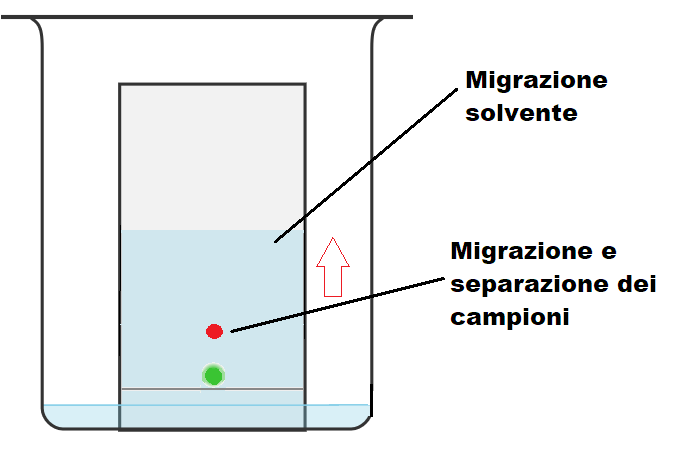
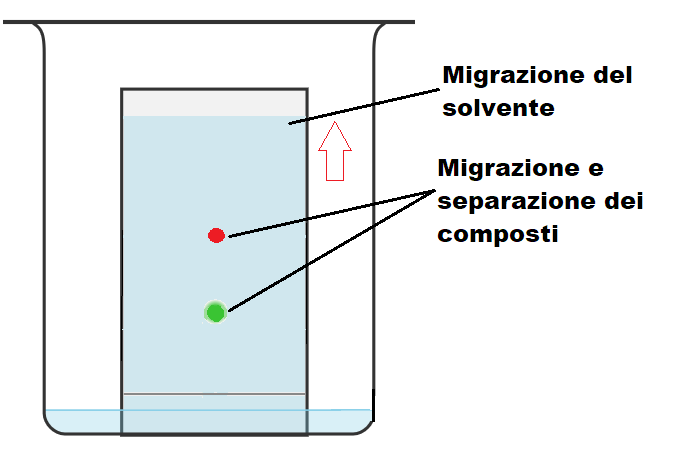
3) Eluire la TLC. Una volta inserito l’eluente e chiusa la camera con il coperchio, si deve attendere che il solvente salga per capillarità lungo tutta la TLC. Durante questa fase il campione migrerà insieme all’eluente ma la sua velocità di migrazione potrà essere diversa. Infatti il campione migrerà molto lentamente quanto più esso interagirà con la fase stazionaria, mentre migrerà tanto più velocemente quanto meno interagirà con la fase stazionaria. Inoltre se il campione puntato su TLC consiste in una miscela di composti, questi si separeranno durante la fase di eluizione perché migreranno con velocità diverse a seconda dell’affinità per la fase stazionaria.
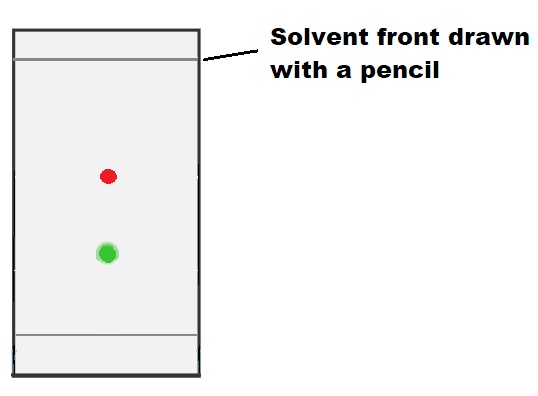
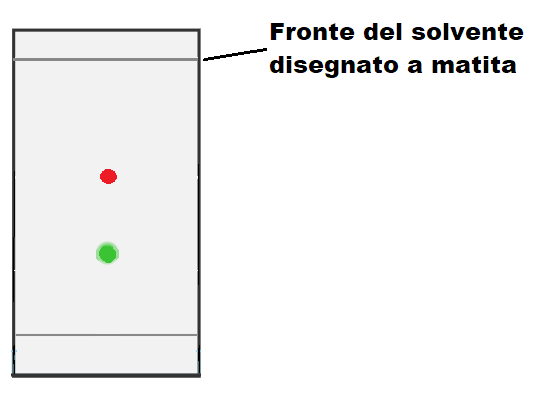
4) Rimuovere la TLC dalla camera eluente quando il solvente è a pochi millimetri dal bordo della TLC, segnare il fronte del solvente con una matita e rivelare la TLC con un’opportuna tecnica.
Le immagini sottostanti chiariscono le tappe sopra descritte, ti basterà scorrere le immagini per vederle tutte.
Fasi stazionarie
Come avrai capito la TLC non può funzionare senza la fase stazionaria (o adsorbente) e la fase mobile (o eluente).
In questo breve paragrafo e nel successivo chiariremo quali fase stazionarie e miscele eluenti esistono e come sceglierle.
Le più comuni fasi stazionarie possono essere classificate in base al loro potere adsorbente come segue:
Forte potere adsorbente: allumina, florisil, gel di silice, carbone attivo;
Medio potere adsorbente: idrossido di calcio, idrossido di magnesio, fosfato di calcio, carbonato di calcio.
Basso potere adsorbente: cellulosa, amido, saccarosio, talco.
L’allumina, ossido di alluminio (Al2O3), è la fase stazionaria con più alto potere adsorbente e la si trova commercializzata in forma basica, neutra e acida. Essa è adatta alla separazione di composti di media e bassa polarità, mentre è sconsigliata per composti molto polari, come ad es. gli acidi carbossilici, perché per via dell’alto potere adsorbente dell’allumina, tali composti potrebbero legarsi irreversibilmente ad essa. Tra le fasi stazionarie elencate certamente la più usata in chimica organica è il gel di silice, un polimero del diossido di silice (SiO2)n. Tale fase stazionaria è usata per separare un’ampia gamma di composti organici tra cui esteri, ammine, composti carbonilici, alcoli, tioli, ecc.
Le fasi stazionarie sopra elencate sono tutte polari, motivo per cui tratterranno di più le sostanze organiche polari. Nell’immagine sottostante sono elencati i composti organici in ordine di affinità crescente per le fasi stazionarie polari.

I composti con maggiore affinità per la fase stazionaria polare, migreranno di meno lungo la TLC, quindi li troveremo come bande basse. Viceversa, le sostanze poco polari sono poco trattenute e migreranno più velocemente con la fase mobile e pertanto saranno eluite per prime.
Miscele eluenti
La miscela eluente è costituita da uno o più solventi con diversa polarità. La miscela eluente più adatta per la nostra TLC sarà quella che consentirà una buona separazione delle bande. In genere la miscela eluente è costituita da un solvente non polare (es. etere di petrolio, esano, cicloesano) e da un solvente più polare (etile acetato, etere dietilico, acetone, ecc.). Una delle miscele più famose, con cui si può sempre iniziare quando si cerca la miscela eluente adatta, è esano/etile acetato in rapporto 8/2. Varie altre combinazioni possono essere provate, variando il rapporto dei due solventi o variando i solventi stessi. Si deve però notare che l’aumento di un solvente polare comporterà una maggiore migrazione delle sostanze organiche polari, mentre una miscela eluente con maggiori quantità di solvente apolare comporta maggiore ritenzione delle bande più polari.
Un aiuto nella scelta della miscela eluente può essere fornito dalla serie eluotropica, una classificazione dei solventi in ordine crescente di potere eluente (vedi figura in basso).

Scopi
Dopo aver visto come funziona una TLC e cosa è la fase stazionaria e la fase mobile, è ora di chiarire quando effettivamente una TLC viene usata in laboratorio.
Di seguito sono elencate le applicazioni più comuni.
Ricerca dell’eluente adatto per la cromatografia su colonna. La cromatografia su colonna serve a purificare grandi quantità di campione e impiega molto solvente. Il suo principio di funzionamento è simile alla TLC, motivo per cui si fanno delle prove ”in piccolo” con le TLC per cercare la miscela eluente adatta per la separazione con colonna cromatografica.
Seguire l’andamento di una colonna cromatografica. Durante la corsa con colonna cromatografica è necessario eseguire molte TLC per comprendere quali frazioni eluite dalla colonna contengano il prodotto desiderato e se esso sia puro.
Seguire lo svolgimento di una reazione. Durante una reazione è possibile effettuare delle TLC di piccole aliquote prelevate dal pallone di reazione per capire se la reazione è conclusa e ha generato il prodotto di interesse.
Controllare la purezza di un composto. Se si carica un composto su TLC e dopo l’eluizione si ottiene una sola banda, generalmente questo implica che il composto è puro.
Riconoscimento di prodotti incogniti. Spesso puntando su TLC un prodotto incognito e uno di riferimento si può vedere se il campione incognito corrisponda a quello di riferimento.
Metodi di rivelazione
Non abbiamo ancora chiarito come visualizzare le bande su TLC dopo l’eluizione. Queste bande, infatti, ad eccezione dei composti colorati, non sono visibili a occhio nudo. Occorrerà quindi un mezzo esterno per vederle. Le tecniche più usate sono elencate di seguito.
Lampada a UV. Questo è il metodo di prima scelta per visualizzare una TLC e solo qualora questo non funzioni si ricorre generalmente agli altri. La lampada a UV per la rivelazione delle TLC è dotata di due lunghezze d’onda: 254 e 366 nm. Quando si attiva la lunghezza d’onda a 254 nm è possibile visualizzare le bande che assorbono nell’UV come macchie scure. Questo avviene perché le TLC sono impregnate con un indicatore fluorescente che a questa lunghezza d’onda emetterà una luce verde, tuttavia nelle zone dove sono presenti i campioni che assorbono nell’UV, tale luce verde non compare e si vedranno, invece, i campioni come bande scure. Diversamente, alla lunghezza d’onda di 366 nm, l’indicatore non è più in grado di emettere la luce verde e, quindi, si potranno vedere tutti quei composti organici che presentano fluorescenza. Dunque a 254 nm si vedranno tutti i composti organici in grado di assorbire nell’UV (composti aromatici, coniugati, ecc.), mentre a 366 nm quelli che presentano fluorescenza.
Metodo universale. Questo metodo funziona con tutti i composti organici e consiste nel spruzzare la TLC, dopo eluizione, con acido solforico concentrato. La lastra viene poi riposta in stufa a 110-120 °C. In queste condizioni tutte le sostanze presenti su TLC saranno ossidate e carbonizzate dando macchie scure visibili.
Uso di reattivi cromogeni. Esistono varie soluzioni di sostanze colorate (cromogeni) che si possono preparare e in cui si possono immergere le TLC. Dopo immersione le TLC vengono asciugate e i composti presenti sono rivelati come bande colorate. Esistono anche cromogeni adatti alla rivelazione di specifici gruppi funzionali. Ad esempio la ninidrina è adatta per la rivelazione degli amminoacidi, il bromocresolo per gli acidi organici, ecc.
Conclusione
In questo articolo, abbiamo affrontato gli aspetti teorici più importanti della TLC.
Se desideri approfondire ulteriormente la TLC, ti offriamo due opzioni:
1) Scarica il file PDF o DOCX qui sotto. Questo documento completo include una guida passo-passo su come eseguire la TLC in laboratorio, un riassunto teorico della TLC, descrizioni della TLC 2D e persino una sezione di risoluzione dei problemi.
2) Unisciti al nostro corso online sulle Tecniche di Laboratorio di Chimica Organica, dove puoi acquisire una conoscenza completa sulle pratiche di laboratorio più comuni. Ogni lezione include video tutorial, spiegazioni teoriche, file di supporto scaricabili e quiz. Dai un’occhiata qui: Laboratorio di Chimica Organica.
Ricordati di votare questo articolo; la tua opinione ci permetterà di migliorare i nostri servizi per te.
Questa lezione

TLC riassunto e guida pratica
€
2.50
Scarica pdf (non modificabile)

TLC riassunto e guida pratica
€
3.50
Scarica docx (modificabile)