Introduzione
In questo articolo vediamo le procedure tipicamente usate in laboratorio per effettuare la reazione di saponificazione.
Prima di iniziare ricordiamo brevemente cos’è questa reazione.
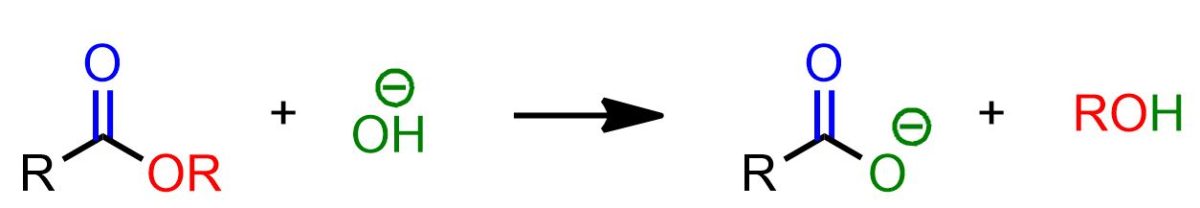
La reazione di saponificazione è l’ idrolisi di un estere mediante impiego di idrossidi.
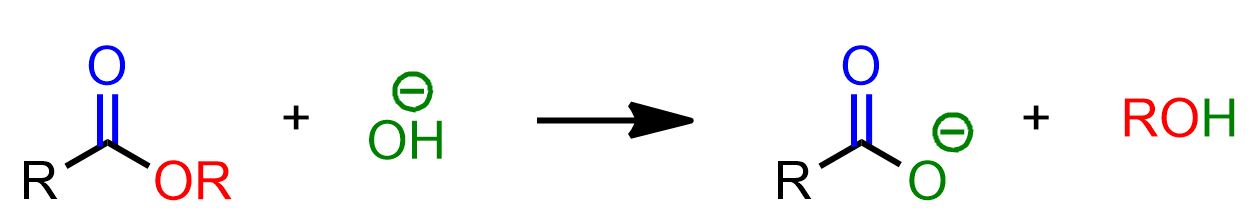
Lo schema in alto mostra la reazione di saponificazione nel suo complesso. Tuttavia tale reazione avviene a più stadi, di cui solo l’ultimo è irreversibile. L’ultimo stadio, infatti, prevede lo scambio acido-base tra l’acido carbossilico e lo ione alcossido. Quest’ultimo passaggio è la driving force di tutta la reazione, che altrimenti sarebbe reversibile.
Generiche condizioni di reazione
Le condizioni tipiche dell’idrolisi basica degli esteri sono:
uso di un eccesso di idrossido;
temperatura ambiente o riflusso .
acidificazione dopo la saponificazione .
Quindi la rezione può essere effettuata a temperatura ambiente o a riflusso, dipendentemente dalla facilità di idrolisi di quel particolare estere.
I solventi più tipici impiegati nella reazione sono quelli alcolici, come MeOH o EtOH, che sono in grado di solubilizzare gli idrossidi. Spesso anche l’acqua è aggiunta per facilitare tale solubilizzazione.
Gli idrossidi più usati sono NaOH e KOH.
Una variante della reazione prevede la catalisi enzimatica mediante le lipasi in acqua.
Tutte le procedure di saponificazione richiedono un ultimo passaggio acido, di solito eseguito aggiungendo HCl alla soluzione acquosa dopo l’estrazione. Questo passaggio è necessario perché, dopo la saponificazione, l’acido carbossilico si trova nella sua forma deprotonata (carbossilato), pertanto è necessario aggiungere un acido per protonarlo.
Procedure tipiche
Dopo aver discusso le caratteristiche generali della saponificazione, vediamo finalmente come eseguire la reazione in laboratorio. Vengono riportate di seguito alcune procedure trovate in letteratura.
Procedure con NaOH come idrossido
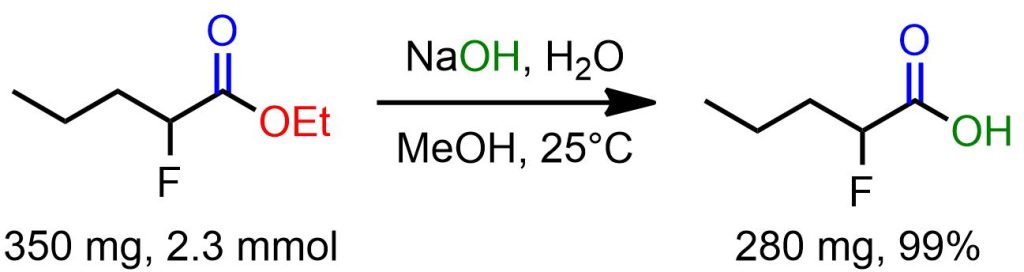
Il 2-fluoropentanoato di etile (350 mg, 2.3 mmol) è stato solubilizzato in una miscela di metanolo (5 ml) e di soluzione acquosa di NaOH 1 M (5 ml). La miscela risultante è stata agitata per 5 ore a temperatura ambiente. Successivamente, HCl (1 M) è stato aggiunto fino a completamento della reazione acida. La miscela è stata estratta con etile acetato (3 x 50 ml). Le fasi organiche combinate sono state lavate con acqua e brine, anidrificate su Na2SO4, filtrate e evaporate a pressione ridotta per dare 250 mg di acido 2-fluoropentanoico (99 % resa) come olio incolore volatile. [1]
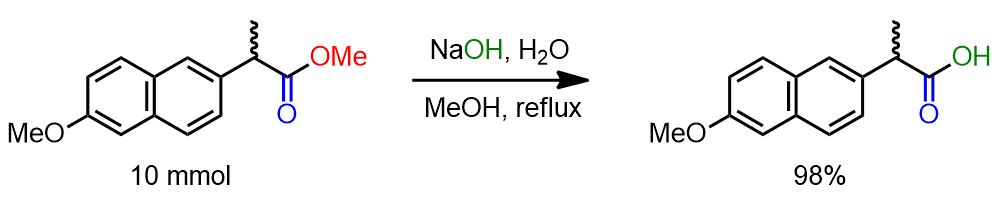
L’ estere è stato dissolto in una soluzione acquosa al 30% di NaOH (15 ml) in MeOH (50 ml) e riscaldato a riflusso sotto agitazione per 4 ore. La miscela di reazione è stata versata in acqua ed estratta con etere etilico (2 x 50 ml). La fase acquosa è stata acidificata con HCl concentrato ed estratta con etere etilico (3 x 80 ml). La fase organica è stata lavata con acqua e anidrificata su Na2SO4 e filtrata. Il solvente è stato rimosso mediante Rotavapor per ottenere l’acido carbossilico (98% resa).[2]
Procedure con KOH come idrossido
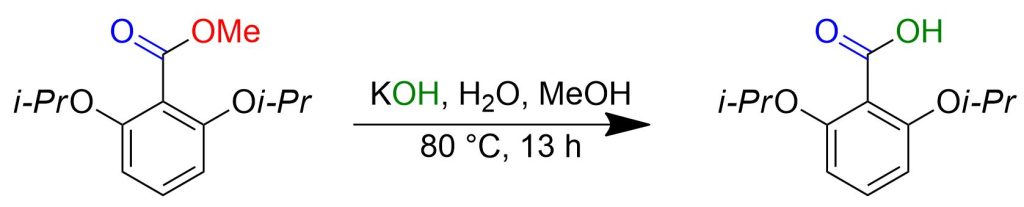
Il potassio idrossido (20 g, 0,36 mol) è stato disciolto in una miscela 9:1, metanolo (90 mL) e acqua (10 mL). A una soluzione di KOH al 20% in peso è stato aggiunto il metile 2,6-diisopropossibenzoato (8,3 g, 0,033 mol), e la miscela è stata riscaldata a 80 °C (temperatura del bagno d’olio). Dopo aver mescolato per 13 ore a 80 °C, la miscela è stata raffreddata a temperatura ambiente, versata in HCl acquoso 1 N ed estratta due volte con etere. Le fasi organiche sono state concentrate a pressione ridotta, e il solido grezzo è stato lavato con esano e asciugato per ottenere l’acido 2,6-diisopropossibenzoico (7,7 g, 0,032 mol) come solido bianco con una resa del 98%.[3]
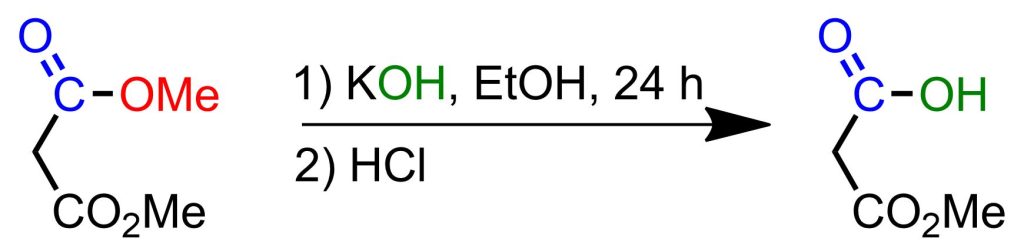
Si aggiunge goccia a goccia 1 mole (132 g) di estere dimetilico dell’acido malonico in 500 ml di etanolo assoluto, a una soluzione di 1 mole di KOH (56 g) in 500 ml di etanolo assoluto. Dopo 24 ore, si filtra il sale di potassio ottenuto, si lava con poco etere e si asciuga sotto vuoto. Si aggiunge goccia a goccia, a una soluzione raffredata con un bagno di acqua e ghiaccio contenente 1 mole di sale di potassio e 100 ml di acqua ghiacciata, 2 moli di HCl concentrato; si estrae 3-4 volte con 100 ml di etere dietilico ciascuna, si anidrifica su solfato di sodio e si distilla il residuo oleoso sotto vuoto. Si ottiene un liquido incolore con resa quasi quantitativa, con punto di ebollizione 84°C/0,18 Torr (letteratura: 168°C/12 Torr).[4]
Procedure con LiOH come idrossido
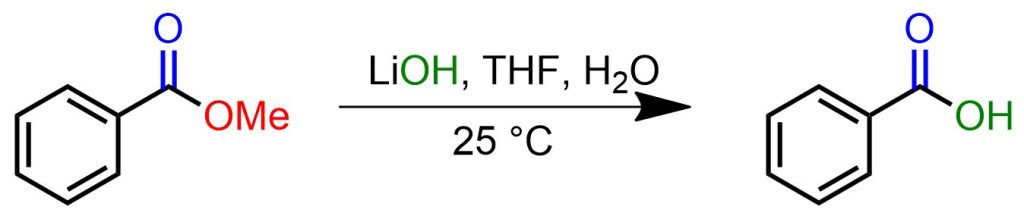
Una miscela di metil benzoato (544 mg, 4 mmol), LiOH (960 mg, 40 mmol) e acqua (4 ml) in THF (20 ml) è stata agitata a temperatura ambiente fino al completamento della reazione (monitorata tramite TLC). La miscela di reazione è stata acidificata con 1 N HCl seguito da estrazione con DCM (2 × 60 ml). Le fasi organiche combinate sono state anidrificate su MgSO4 anidro e concentrate sotto vuoto per ottenere il’acido benzoico puro (88%).[5]
Procedure con lipasi
Esempio di risoluzione cinetica enzimatica.
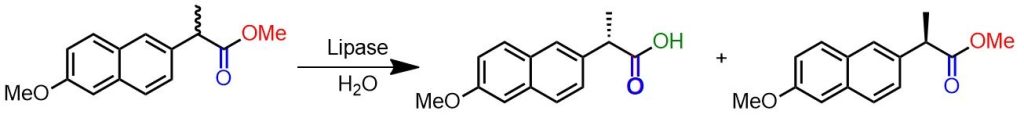
Naprossene metil estere racemico finemente suddiviso in polvere (244 mg, 1,0 mmol), mercaptoetanolo (1 μmol) e alcol polivinilico (10 mg) vengono aggiunti alla lipasi grezza di C. cylindracea (Sigma L1754 Type VII, 600 μg proteina) in una soluzione di tampone fosfato 0,2 M a pH 8,0 (1 ml). La sospensione viene agitata a 22°C per 42 h. La miscela di reazione è centrifugata a 1000 rpm per 5 min, il precipitato è lavato con un tampone fosfato 0.2 M a pH 8 e poi nuovamente centrifugato per raccogliere l’enantiomero non reagito insolubile in acqua. Il surnatante e la fase acquosa sono combinate e acidificate con HCl (3 N) a pH 2. Il precipitato è recuperato mediante filtrazione per dare l’enantiomero trasformato in acido carbossilico. [6]
Riferimenti
[1] Chen, X., Decker, M., Higuchi, T., & Hoffmann, M. (2019). Sartan analogue. WO2019134765A1
[2] Castaldi, G., Belli, A., Uggeri, F., & Giordano, C. (1983). A Lewis acid catalyzed 1,2 aryl shift in .alpha.-haloalkyl aryl acetals: a convenient route to .alpha.-arylalkanoic acids. Journal of Organic Chemistry, 48(24), 4658–4661. https://doi.org/10.1021/jo00172a041
[3] Gao, Q., Ishihara, K., Maruyama, T., Mouri, M., & Yamamoto, H. (1994). Asymmetric hetero Diels-Alder reaction catalyzed by stable and easily prepared CAB catalysts. Tetrahedron, 50(4), 979–988. https://doi.org/10.1016/s0040-4020(01)80812-7
[4] Dallacker, F., & Schubert, J. (1975). Derivate des Methylendioxybenzols, 39. Über Polyencarbonsäureimide des Methylendioxybenzols. Chemische Berichte, 108(1), 95–108. https://doi.org/10.1002/cber.19751080113
[5] De, S. K. (2021). Applied Organic Chemistry: Reaction mechanisms and experimental procedures in medicinal chemistry. https://openlibrary.org/books/OL29476874M/Applied_Organic_Chemistry.
[6] Gu, Q., Chen, C., & Sih, C. J. (1986). A facile enzymatic resolution process for the preparation of (+)–2-(6-hethoxy-2-naphthyl)propionic acid (Naproxen). Tetrahedron Letters, 27(16), 1763–1766. https://doi.org/10.1016/s0040-4039(00)84368-3.